- 大分類
-
- 凝固
- 小分類
-
- 分子
プロテインS protein S
解説
【概要】
プロテインS(protein S: PS)はビタミンK依存性タンパク質で、主に肝細胞と血管内皮細胞で合成されるが、血管平滑筋細胞、巨核球、マクロファージ、T細胞、Leydig細胞、骨芽細胞など様々な細胞が産生する。PS 遺伝子(PROS1)は第3染色体のセントロメア近く(3q11.1)に位置し、全長約100 kbで15個のエクソンからなるが、近傍(3p11.1)には偽遺伝子(PROS2P)が存在する。
【分子量、半減期、血中濃度】
成熟PSタンパク質の分子量は73 kDa(635個アミノ酸)である。血漿中PS濃度は約350 nM(25 µg/mL)で、約60%は補体活性化(古典経路)の制御因子であるC4b結合蛋白質(C4b binding protein: C4BP)と複合体を形成し、残りの約40%が遊離型として存在する。血漿中C4BP濃度は約250 nMで、約80%はα鎖7個とβ鎖1個がS-S結合した構造(α7β1)だが、その他にα鎖7個のみ(α7β0)、α鎖6個とβ鎖1個(α6β1)のアイソフォームが存在する。Ca2+存在下ではPSはsex-hormone-binding globulin(SHBG)様領域を介して β鎖に強い親和性(Kd: 0.1 nM)で結合するため、C4BPβ+に結合できなかったPSが遊離型となる。急性炎症時にはC4BPα鎖の合成が亢進するため、β鎖を有しないC4BPβ–の血中濃度が上昇するが、C4BPβ+とPSの上昇は軽度であり遊離型PS濃度は変化しない。PSの血中半減期は約40時間で、プロテインC(PC)や第VII因子の半減期(5〜6時間)に比べると長い。
【構造と機能】
NH2末端から γ-carboxyglutamic acid(Gla)ドメイン、thrombin-sensitive region(TSR)、4個の連続するepidermal growth factor(EGF)様ドメイン(EGF1-EGF4)、2個のラミニンGドメイン(LG1, LG2)が連続するSHBG様領域からなる(図)。PSの機能としては、(1) 活性化プロテインC(activated protein C: APC)コファクター活性:PSはAPCによる活性化第V因子(FVa)のArg306切断を促進し完全に失活化し、活性化第VIII因子(FVIIIa)の失活化をFVとともに相乗的に促進する。(2)組織因子経路インヒビター(tissue factor pathway inhibitor: TFPI)コファクター活性:PSはTFPIαのKunitz-3ドメインに結合してKunitz-2ドメインによる活性化第X因子(FXa)阻害をFVとともに相乗的に促進する。(3) APC/TFPI非依存的抗凝固活性:PSはprothrombinase複合体、内因性FXase複合体に直接結合して阻害する。(4)受容体型チロシンキナーゼTAMファミリーのリガンドとして細胞機能制御:PSおよび類似体のgrowth arrest-specific gene 6(Gas6)はSHBG様領域を介して細胞膜上のTAMファミリー(TYRO3、AXL、MERTK)に結合し、免疫、神経、生殖、血管など様々な臓器の恒常性維持に関与する。なお、PSはGas6と異なりAXLには結合しない。
遊離型PSのみが(1)と(2)のコファクター活性を示し、 (1)と(4)の機能発現には、Glaドメインを介した細胞膜リン脂質のフォスファチジルセリンへの強い親和性が関与する。
【ノックアウトマウスの表現型】
【病態との関わり】
先天性PS欠乏症では、PROS1の変異によりPSの血液凝固制御活性が低下し、若年性に静脈血栓塞栓症(venous thromboembolism: VTE)を発症する。I型PS欠乏症(PS発現低下)のホモ接合体や複合ヘテロ接合体で血中PS濃度が著しく低下している場合、新生児期に致死的な電撃性紫斑病を発症するが、PC欠乏症に比べると報告例は少ない。遺伝性PS欠乏症の頻度は欧米白人に比べて日本人では著しく高いが、その原因の一つとして、PS発現は低下していないがAPCコファクター活性が低下する(II型PS欠乏症)PS Tokushima変異(p.Lys196Glu, rs121918474)の存在が考えられる。PS Tokushima変異のヘテロ接合体は日本人健常者の1.3-1.8%に存在し、 VTEのリスクを3.7-8.6倍上昇させる。 血中PS濃度は閉経前女性で低く、妊娠中・産褥期、エストロゲン含有経口避妊薬やエストロゲン製剤内服時にはさらに低下するためVTE発症のリスクが高まる。
なお、TFPIコファクター活性、APC/TFPI非依存的抗凝固活性、TAMファミリーのリガンドとしての細胞機能制御活性の先天性機能異常をきたした症例はまだ報告されていない。
図表
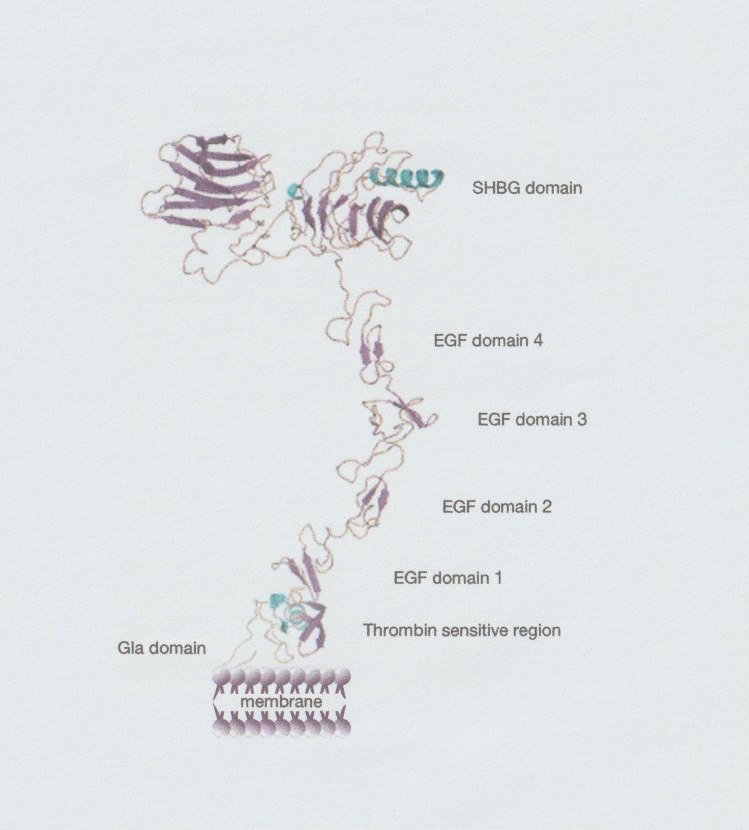
図. ヒトプロテインSの構造モデル(細胞膜上) : 参考文献4)より引用
引用文献
1) Saller F, et al: Generation and phenotypic analysis of protein S-deficient mice. Blood 114:2307-14, 2009.
3) Calzavarini S, et al.: Platelet protein S limits venous but not arterial thrombosis propensity by controlling coagulation in the thrombus. Blood 135: 1969-82, 2020.
参考文献
1) 津田博子:ビタミンK依存性タンパク質プロテインS –機能と病態との関連-. 日本血栓止血学会誌, 30 (4): 642-651, 2019.
2) Dahlback, B.: Vitamin K-Dependent Protein S: Beyond the Protein C Pathway., Semin Thromb Hemost., 44:176-184, 2018.
3) Burstyn-Cohen T, et al.: TAM receptors in phagocytosis: Beyond the mere internalization of particles., Immunological Reviews, 319:7-26, 2023.
4) 津田博子. プロテインC、プロテインS、血管内皮プロテインCレセプターの基礎と臨床. In: 一瀬白帝, 丸山征郎, 和田英夫編, 新・血栓止血血管学 –抗凝固と線溶-: 金芳堂; 2015:22-30.
