- 大分類
-
- 凝固
- 小分類
-
- 分子
ポリリン酸 polyphosphate
解説
【構造】
DNA合成酵素の研究で広く知られるArthur Kornberg博士はノーベル賞を受賞した後、大腸菌のポリリン酸の研究を精力的に行った(1)。進化的な観点からみると、ポリリン酸は原核生物および真核生物に普遍的に存在する。原核細胞ではポリリン酸はポリリン酸キナーゼ(polyphosphate kinase)により合成されるが(1)、哺乳類のポリリン酸の合成系は同定されていない。血栓止血領域でのポリリン酸の役割は、2006年にMorrissey博士らのグループにより報告され(2)、現在その重要性は揺るぎないものになっている。
ポリリン酸は無機リン酸が直鎖状につながった陰電荷物質である。ポリリン酸は血小板の濃染顆粒や微生物内部の顆粒中に蓄えられており、刺激依存性に放出される。血小板は60-100個のリン酸が結合した中鎖ポリリン酸を含み、原核生物の顆粒中には数百個–数千個のリン酸がつながった長鎖ポリリン酸が存在する。
【凝固系・キニン系・補体系における機能】
ポリリン酸は内因系凝固反応の惹起因子であり、凝固第XII因子(FXII)を自己活性化するとともに、FXIIとプレカリクレインの相互活性化を促進する。活性化されたFXII(FXIIa)は、凝固第XI因子(FXI)を活性化することで凝固反応を進める。プレカリクレインの活性型である血漿カリクレインは高分子キニノーゲンを切断しブラジキニンを遊離する。ポリリン酸のこの内因系凝固反応の活性化能は鎖長に依存し、長鎖ポリリン酸はその作用が強いが、血小板が放出する中鎖ポリリン酸は弱い。しかし、活性化した血小板膜には長鎖ポリリン酸を含む粒子が結合し、この長鎖ポリリン酸が内因系凝固反応の活性化を行うとの報告がある(3)。また、血小板が放出する中鎖ポリリン酸は、トロンビンによるFXIと凝固第V因子(FV)の活性化を著しく促進する。ポリリン酸はフィブリンに取り込まれ、太く強固な繊維を形成し線溶系に抵抗性を示す。このように、ポリリン酸は血栓促進因子として際立った特徴を持つ。マウスを用いた研究では、ポリリン酸-FXII経路により凝固系とキニン系が作動することが明らかになっており、マウスにポリリン酸を静注すると血管透過性が亢進し、かつ致死的肺塞栓が観察される(4)。一方、補体系に対しては、ポリリン酸は抑制的に働く。すなわち、C1インヒビターによるC1s活性阻害を亢進し、補体C5b,6複合体を不安定化する。
【病態との関わり】
血小板の濃染顆粒にはADPやポリリン酸などの血栓惹起物質が含まれており、血小板の濃染顆粒を含むリソソーム関連小器官が欠損したHermansky-Pudlak症候群(HPS)の患者では、幼少時より軽度から中等度の出血傾向を認める。HPS患者ではポリリン酸の貯蔵部位である血小板濃染顆粒が欠損するため、血小板の活性化に伴うポリリン酸の放出は認められない(4)。ポリリン酸は脱リン酸化酵素で容易に分解を受け、血中半減期は1.5-2時間である。Xenotropic and polytropic retrovirus receptor 1(XPR1)はリン酸を排出するトランスポーターであるが、血小板でこの遺伝子を欠損したマウスは血小板ポリリン酸が増加し、静動脈血栓症が亢進した(5)。
【その他のポイント・お役立ち情報】
ポリリン酸は抗血栓療法の標的分子と考えられている。活性を中和する低分子化合物はマウス血栓モデルで強力な抗血栓能を示した(6)。大腸菌のポリリン酸分解酵素(exopolyphosphatase)はマウス血栓モデルで抗血栓能を示した(7)。
図表
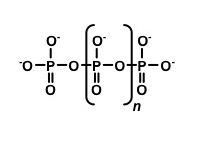
ポリリン酸の化学構造
引用文献
(1) Rao NN, Gómez-García MR, Kornberg A. Inorganic polyphosphate: essential for growth and survival. Annu Rev Biochem, 78: 605–647, 2009.
(2) Smith SA, Mutch NJ, Baskar D, et al. Polyphosphate modulates blood coagulation and fibrinolysis. Proc Natl Acad Sci USA, 103: 903–908, 2006.
(3) Verhoef JJ, Barendrecht AD, Nickel KF, et al. Polyphosphate nanoparticles on the platelet surface trigger contact system activation. Blood, 129:1707-1717, 2017.
(4) Muller F, Mutch NJ, Schenk WA, et al. Platelet polyphosphates are proinflammatory and procoagulant mediators in vivo. Cell, 139: 1143-1156, 2009.
(5) Mailer RK, Allende M, Heestermans M, et al. Xenotropic and polytropic retrovirus receptor 1 regulates procoagulant platelet polyphosphate. Blood 137: 1392-1405, 2021.
(6) Jain S, Pitoc GA, Holl EK, et al. Nucleic acid scavengers inhibit thrombosis without increasing bleeding. Proc Natl Acad Sci USA, 109: 12938-12943, 2012.
(7) Labberton L, Kenne E, Long AT, et al. Neutralizing blood-borne polyphosphate in vivo provides safe thromboprotection. Nat Commun, 7:12616, 2016.
参考文献
Baker CJ, Smith SA, Morrissey JH. Polyphosphate in thrombosis, hemostasis, and inflammation. Res Pract Thromb Haemost 3: 18-25, 2018.
Mailer RKW, Hänel L, Allende M, Renné T. Polyphosphate as a target for interference with inflammation and thrombosis, Front Med (Lausanne) 12; 6: 76, 2019.
