- 大分類
-
- 凝固
- 小分類
-
- 薬剤
フォンダパリヌクス fondaparinux
解説
【概要】
静脈血栓塞栓症(venous thromboembolism: VTE)は、深部静脈血栓症(主に下肢の深部静脈に血栓ができる病態:deep vein thrombosis: DVT)と肺塞栓症(深部静脈に形成された血栓が肺動脈に飛んで肺動脈が塞がれ、重篤な場合死に至る疾患、pulmonary embolism:PE)といった一連の病態の総称である。
本剤は、2001 年12 月に優先審査により米国で下肢整形外科手術施行患者におけるVTE予防薬として承認されて以来、下肢整形外科手術施行患者におけるVTE予防に係る効能で世界94ヵ国以上、腹部手術施行患者におけるVTE予防に係る効能で世界66 ヵ国、急性PE 及び急性DVT の治療に関する効能・効果で世界64カ国で承認されている。
国内では、アリクストラ皮下注1.5mg及び2.5mgについて2005年11月に承認申請を行い、優先審査により2007年4月に「VTE の発現リスクの高い、下肢整形外科手術施行患者におけるVTEの発症抑制」に対して承認された。また、優先審査により2008 年5月には腹部手術施行患者に適応が追加された。さらに、2007年以降よりアリクストラ皮下注5mg及び7.5mgについて「急性PE患者及び急性DVT患者の治療」に関する第Ⅲ相試験が開始され、初期治療における本剤の有効性及び安全性が確認されたため海外臨床試験の成績と合わせ、治療用薬剤として承認申請を行い、2011年1月に承認されている。
【一般名(製品名)】
フォンダパリヌクスナトリウム(アリクストラ)
【作用機序】
フォンダパリヌクスナトリウム(アリクストラ)は完全化学合成により得られた分子量1728.08の硫酸ペンタサッカライドのナトリウム塩で、アンチトロンビン(antithrombin: AT)に選択的かつ特異的に結合し、ATの抗第Xa因子活性を増強することにより、トロンビン生成を阻害し、フィブリン形成を抑制する抗凝固薬である(図1))。
【半減期・代謝経路】
日本人健康成人男性に本剤を単回皮下投与した場合、投与後約2時間で最高血中濃度に達し、消失半減期は約14~17時間である。なお、代謝経路は主として腎臓から尿中に排泄される。
【適応】
1.予防投与の効能又は効果
「静脈血栓塞栓症の発現リスクの高い、次の患者における静脈血栓塞栓症の発症抑制」
・下肢整形外科手術施行患者
・腹部手術施行患者
用法及び用量としては、通常、成人には、2.5mgを1日1回皮下投与する。なお、腎障害のある患者に対しては、腎機能の程度に応じて1.5mg 1 日1 回に減量する。クレアチニンクリアランス20~30mL/minの患者では、1.5mgを1 日1 回、クレアチニンクリアランス30~50mL/min の患者では2.5mg あるいは出血の危険性が高いと考えられる場合には1.5mg を1 日1 回皮下投与する。
なお、下肢整形外科手術施行患者では15日間以上、腹部手術施行患者では9日間以上投与した場合の有効性及び安全性は、国内臨床試験においては検討されていない。
2.治療投与の効能又は効果
「急性肺血栓塞栓症及び急性深部静脈血栓症の治療」
ショックや低血圧が遷延するような血行動態が不安定な患者又は血栓溶解剤の使用や肺塞栓摘出術が必要な患者に対する有効性及び安全性は確認されていない。
用法及び用量としては、通常、成人には以下の用量を1日1回皮下投与する。体重50kg未満:5mg、体重50~100kg:7.5mg、体重100kg超:10mg。
図表
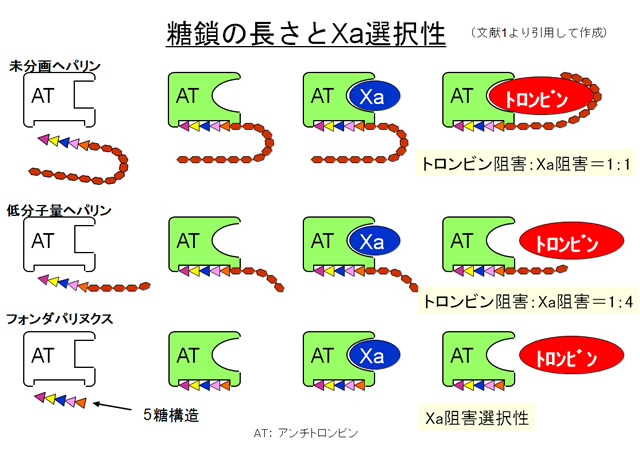
フォンダパリヌクス
参考文献
1) Wong NN: Fondaparinux: a synthetic selective factor-Xa inhibitor. Heart Dis 5: 295
